مولکول های افلاطونی چه هستند؟

مولکول های افلاطونی متقارنترین مولکولهایی به شمار میآیند که از ترکیب کربن و هیدروژن ایجاد میشوند و در حقیقت، هیدروکربنهایی سهبعدی با زیباییهای تقارنی هستند. این مولکولها که با الهام از «اجسام افلاطونی» کشف یا ساخته شدهاند اغلب به خاطر کشش و فشار بالایی که در آنها وجود دارد، شکلهای پیوندی غیرعادی و خواص شیمیایی متفاوت و جدیدی از خود نشان میدهند. در ادامه، با جزئیات این مولکول های افلاطونی بیشتر آشنا میشویم.
جسم افلاطونی چیست؟
در هندسه فضایی، به چندوجهیهای منتظمِ محدب به اصطلاح «جسم افلاطونی» گفته میشود. به عبارت دیگر، اجسام افلاطونی چندوجهیهايی محدب و منظم هستند كه خصوصيات اصلی آنها برابر بودن زوايا و يکسان بودن طول اضلاع وجوه و يالهای آنهاست. در فضای سهبعدی و به هنگام بررسی مولکول های افلاطونی میتوان نشان داد که تنها پنج جسم افلاطونی وجود دارد و این اجسام عبارتند از:
- چهاروجهی منتظم، متشکل از چهار مثلث متساویالاضلاع
- ششوجهی منتظم (مکعب)، متشکل از شش مربع
- هشتوجهی منتظم، متشکل از هشت مثلث متساویالاضلاع
- دوازدهوجهی منتظم، متشکل از دوازده پنجضلعی منتظم
- بیستوجهی منتظم، متشکل از بیست مثلث متساویالاضلاع

سابقه آشنايی با اين اجسام به يونان باستان باز میگردد. ریاضیدانان یونانی با خواص هندسی آنها به خوبی آشنا بودند و به خاطر تقارنشان، آنها را اجسامی كامل تلقی میکردند. پس از آنکه افلاطون هر یك از عناصر كلاسیك (اربعه) يعنی خاک، هوا، آب و آتش را به يکی از اين اجسام نسبت داد و نظراتش را در اينباره در دوران سالخوردگیاش (در كتاب مكالمه «تيماﺋوس» (Timaeus) و در قالب نقل داستان آفرینش) شرح داد، اين نامگذاری شكل گرفت. مدتی بعد، ارسطو عنصر پنجم يعنی «اثير» را معرفی کرد و آن را به دوازهوجهی نسبت داد.
با اینکه بر خلاف آرای افلاطون، اجسام افلاطونی واحدهای ساختاری هستی نیستند؛ اما همانطور که در ابتدای مطلب و در معرفی مولکول های افلاطونی اشاره کردیم، هیدروکربنهای افلاطونی نمایش مولکولی این اجسام هستند. در این مولکولها، رأسها با اتمهای کربن و اضلاع با پیوند کربن-کربن جایگزین شدهاند.
چهاروجهیهای تتراهدران، نخستین جسم افلاطونی
از بين پنج جسم افلاطونی، چهاروجهی سادهترين جسم است که گونه شيميايی معادل آن با فرمول $$C_4H_4$$، «تتراهدران» نامگذاری شده است. اما سادگی کار همینجا تمام میشود. اگرچه تلاشهای زيادی برای سنتز (ساخت) اين تركیب صورت گرفته اما اين تلاشها تا کنون موفقیتآمیز نبوده است. به نظر میرسد از آنجاییکه این مولکول تحت «کشش زاویهای» (Angle Strain) قابل توجهی قرار دارد، تحت شرايط عادی آزمايشگاه به اندازه كافی پايدار نيست و همین باعث به بنبست رسیدن تلاشها بوده است.
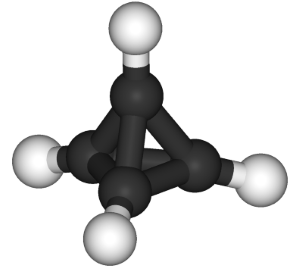
با وجود شکست در ساخت تتراهدران هیدروکربنی، مشتقاتی از تتراهدران با موفقيت سنتز شدهاند كه در آن به جای اتمهای هيدروژن، گروههای بزرگتری با ویژگی پايداركنندگی قرار گرفتهاند. از جمله این مولکولها میتوان به مشتقاتی كه هيدروژنهای آنها با چهار گروه «بوتيل نوع سوم» يا چهار گروه «تریمتيلسيليل» (Trimethylsilyl) جايگزين شدهاند، اشاره كرد كه به صورت جامدات پايدار جداسازی شدهاند.
در حالتی كه مشتق تریمتيلسيليل داشته باشيم، پيوندهاي كربن-کربن (C-C) این مولکول به طور مشخص كوتاهتر از طول معمول پيوندهای C-C خواهد شد. اين تركیب علاوه بر اين میتواند دوپار (ديمر) شود و به شكل تركیب دیهدران درآيد كه در آن دو چهاروجهی با پيوندی حتی كوتاهتر به یکدیگر متصل شدهاند.
در حالت کلیتر، اصطلاح تتراهدران برای توصیف گروهی از مولکولها و یونهای چهاروجهی با ساختاری مشابه نیز استفاده میشود. برای مثال، فسفر سفيد از چهار وجهیهای $$P_4$$ ساخته شده است. همچنين سنتز گونهای مشابه با تتراهدران از چهاروجهیهای سیلیسیم ($$Si_4$$) با شاخههايی از گروههای پايداركننده سيليل (نظير $$H_3Si$$ يا مشتقات آن) گزارش شده است.
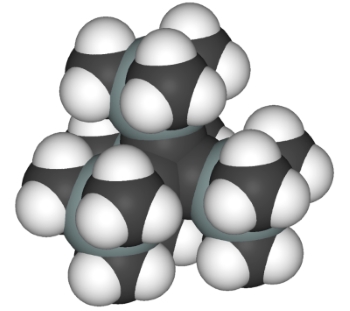
مکعبهای کوبان، دومین جسم افلاطونی
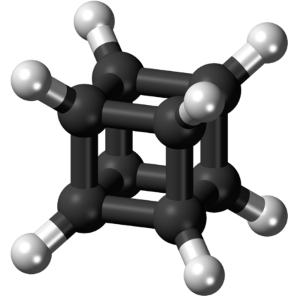
در بررسی مولکول های افلاطونی باید اشارهای هم به مکعبهای کوبان داشته باشیم. مکعب دومين جسم افلاطونی است که هیدروکربن معادل آن «کوبان» (Cubane) نام دارند و از سال 1964 برای شیمیدانان شناخته شده است. كوبان، جامدی پايدار است که در دمای 131 درجه سلسیوس ذوب ميشود.
چگالی کوبان ۱/29 گرم بر سانتیمترمکعب است كه برای یک مولکول هیدروکربنی چگالی بالایی محسوب میشود. با توجه به سنتز گونههای نيتراته شده کوبان كه در آنها بين چهار تا هشت هيدروژن با گروههای نيترو جايگزين شدهاند، كوبان، شيمی غنيتری پیدا کرده است. ترکیبات مذکور انرژی بسيار بالايي دارند و میتوان به عنوان مواد منفجره از آنها استفاده کرد.
ساختارهايي از نوع كوبان در طبيعت به وفور يافت ميشوند. از جمله این مواد میتوان به پروتئینهای آهن-گوگرد اشاره کرد که ساختار مكعبی دارند و هر یک از کنجهای مکعب به طور یکی در میان، با اتمهای آهن و گوگرد اشغال شده است.
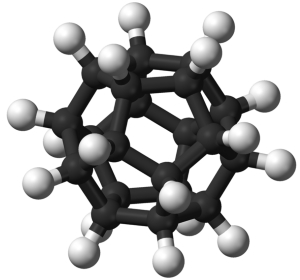
دوازدهوجهیهای دودکاهدران، سومین جسم افلاطونی
سومين جسم افلاطونی یک دوازدهوجهی است. این جسم «دودكاهدران» (Dodecahedrane) با فرمول شیمیایی $$C _ {20} H _ {20}$$ و وجوه پنج ضلعی است که در طبیعت به شکل عادی یافت نمیشود و برای نخستین بار در سال 1982 سنتز شد. در این مولکول، هر اتم کربن با سه اتم کربن همسایه و یک اتم هیدروژن پیوند برقرار کرده است. بررسی ساختار این مولکول با طيفسنجی «رزونانس مغناطیسی هستهای» (NMR) نشان داد تمام اتمهای كربن و همه اتمهای هيدروژن آن از لحاظ تقارنی معادل هستند و با یکدیگر تفاوتی ندارند.
یکی از ویژگیهای جالب دودکاهدران وقتی خودنمایی میکند که آن را با یونهای هلیم بمباران کنیم. در این حالت، كسري از مولكولها به شكل تركیبی درمیآیند که از لحاظ شیمیایی با نماد $$He@C_{20} H_{20}$$ نشان داده میشوند و بیانگر این هستند كه هليم با پيوند شيميايی به دودكاهدران متصل نشده بلكه درون حفره این مولکول به دام افتاده است و از لحاظ فيزیكی قادر به فرار از قفس كربن نيست.
مولکول های افلاطونی و مولکولهای غیرممکن
اگر از ابتدای مطلب به یاد داشته باشید، پنج جسم افلاطوني در فضای سهبعدی وجود دارند؛ بنابراین هنوز دو ساختار هشتوجهی و بيستوجهی باقیماندهاند که مولکول های افلاطونی آنها را معرفی نکردهایم. دلیل موضوع ساده است؛ سنتز این مولکولها عملا غیرممکن است. در «اُكتاهدران» (تركیبي هشتوجهي با فرمول $$C_6$$) به نظر میرسد كشش بسيار زيادی وجود دارد و با ترکیبی به شدت ناپایدار مواجه هستیم.
از يك سو اندازه زوايای بين پيوندها بسيار كوچك هستد و از سویی ديگر، بر خلاف تتراهدران نمیتوان گروههای پايداركننده را به اتمهای كربن متصل كرد زیرا هر چهار والانس (ظرفیت) هر یك از اتمهای كربن درگير پيوند با چهار اتم كربن ديگر هستند. به طور مشابه، ساخت یک بيستوجهی از اتمهای كربن امکانپذیر نیست، زیرا در ساختار هندسی بيستوجهی، هر كنج با پنج يال به كنجهای همسايه متصل است و كربن از نظر ظرفیتی توانايی برقراری پنج پيوند را ندارد.